|
NÉV: SZILÍCIUM
(silex = "kovakő”)
KÉMIAI JEL:
Si
ANYAGSZERKEZET:
rendszám = 14
a.: ATOMSZERKEZET: 14
p+, 14 e–, 14 n0, 3 e–-héj, 4
külső e–
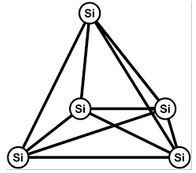
b.: HALMAZSZERKEZET:
Kovalens kötésű, piramis alakú
térrács
1 mol
tömege = 28 gramm
|
 |
FIZIKAI TULAJDONSÁGOK:
Szürke színű, fémesen csillogó, nagyon
kemény anyag. Az áramot egy irányba vezeti (félvezető).

0
KÉMIAI TULAJDONSÁGOK:
Oxigénnel egyesülve szilícium-dioxiddá
ég el:
Si + O2
®
SiO2
A szilíciumot tartalmazó sav a kovasav
(H2SiO3)
A szilícium nem mérgező anyag.
ELŐFORDULÁS:
Elemi állapotban ritka.
Vegyületei viszont nagyon gyakoriak. A szilikátok a földkéreg
leggyakoribb kőzeteit alkotják. (azbeszt, kovaföld)
A szilícium-dioxid a homok,
a természetes kvarc alkotója. A kvarc nagyon kemény, ellenálló, oldhatatlan
ásvány. Nagyméretű kristályai féldrágakövek (hegyikristály, ametiszt, opál).
Előfordul egyes kovamoszatok vázában és a
szem üvegtestjében.
ELŐÁLLÍTÁS:
A szilícium-dioxidot magnéziummal redukálják.
FELHASZNÁLÁS:
Az informatikai iparban a számítógépek processzorait (CPU)
és egyéb chipjeit szilícium lapkák alkotják. A kohászatban is fontos
szerepet tölt be: korrózióálló acélok előállításához használják
ötvözőanyagként. A szilícium-dioxid nagy részét üveggyártásra, vagy
ékszerkészítésre használják.
ÉRDEKESSÉGEK:
Egy átlagos ember testében 1,4 g szilícium található
meg. Legnagyobb részt a kötőszövetben, de előfordul a csontokban, a
porcokban, a bőrben, a visszerekben, a verőerekben, az inakban és a szem
szaru- és ínhártyájában. A kötőszövet felépítésében játszik fontos szerepet.
Megfelelő mennyiségű jelenléte a bőr, a haj és a köröm egészségéhez
szükséges.
Vissza
|

