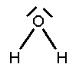
VÍZ (HIDROGÉN-OXID) KÉMIAI JEL: H2OANYAGSZERKEZET: O: 8 p+, 8 e–, 8 n0, 2 e–-héj, 6 külső e– b., HALMAZSZERKEZET:
FIZIKAI TULAJDONSÁGOK: Színtelen, szagtalan, íztelen folyadék. Sűrűsége 1 g/cm 3.Olvadáspont: 0 oC, forráspont: 100 oC. Nagyon jó oldószer, elsősorban az ionkristályos vegyületeket és a dipólus molekulájú anyagokat oldja jól. KÉMIAI TULAJDONSÁGOK: Mivel égéstermék, nem éghető, sőt az egyik legjobb tűzoltó szer. Mivel a molekula a reakciópartnertől függően képes H +-ion (p+) felvételére és leadására is, kémiailag amfoter jellemű.a.: A savmolekuláktól protont képes átvenni, ezért bázisként
viselkedik: Az oldat az oxonium-ionok (H3O+) túlsúlya miatt savas kémhatású. b.: Bizonyos molekuláknak protont képes leadni, ezért savként viselkedik: Az oldat a hidroxid-ionok (OH–) túlsúlya miatt lúgos kémhatású. c.: A tiszta desztillált víz azonos mennyiségben tartalmaz oxonium- és
hidroxid-ionokat, ezért semleges kémhatású: A nagyon kis elektronvonzó képességű fémek a vizet bontják, hidrogéngáz fejlődik, és a keletkező OH –-ionoktól az oldat lúgos kémhatású lesz:2 Na + 2 H2O ® 2 NaOH + H2 A tiszta víz nem mérgező, és az élet nélkülözhetetlen feltétele. ELŐFORDULÁS: Tiszta víz a természetben mint vízgőz (felhők) és csapadék (jég, hó, eső) található. A víz leggyakrabban különböző oldatokat alkot (tengervíz, édesvizek, ásványvizek). Nélkülözhetetlen alkotója az élő szervezeteknek, és kristályvízként bizonyos ásványokban (gipsz) megtalálható. ELŐÁLLÍTÁS: a.: Laboratóriumban hidrogén égetésével állítják elő: b.: Az ipar számára szükséges vizet a tengerekből, folyókból, tavakból nyerik, vagy kutakat fúrnak. FELHASZNÁLÁS: Ivóvízként*, a leggyakrabban használt oldószer (mosás), ipari vízként (hűtővíz a hő- és atomerőművekben, áramtermelésre), a mezőgazdaságban öntözésre, fontos vegyipari nyersanyag (savak, műtrágyák előállításához). ÉRDEKESSÉGEK: * A világon naponta kb. 8 milliárd m3 ivóvíz fogy
|